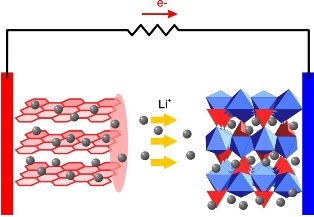
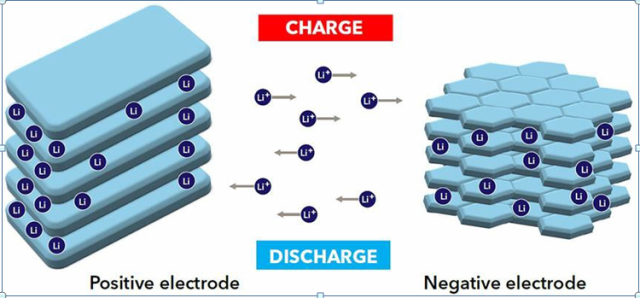
Принцип работы любого электрического аккумулятора заключается в накоплении электрической энергии в процессе химической реакции, происходящей при протекании через аккумулятор зарядного электрического тока, и генерации электрической энергии при протекании разрядного тока в процессе обратной химической реакции.
Обратимость химической реакции в аккумуляторе позволяет многократно разряжать и заряжать аккумулятор. В этом и заключается преимущество аккумуляторов перед одноразовыми источниками тока, обычными батарейками, в которых возможен лишь разрядный ток.
В качестве среды для переноса заряда с одного электрода аккумулятора на другой, используется электролит – специальный раствор, благодаря химической реакции которого с материалом на электродах становятся возможными как прямая, так и обратная химические реакции в аккумуляторе, что и делает возможным как заряд аккумулятора, так и его разряд.
Сегодня одним из наиболее перспективных типов аккумуляторов является литий-ионный аккумулятор. В этих аккумуляторах в качестве отрицательного электрода (катода) выступает алюминий, а в качестве положительного электрода (анода) – медь. Электроды могут иметь различную форму, как правило, это фольга в форме цилиндра или продолговатого пакета.
На алюминиевую фольгу наносят катодный материал, которым чаще всего может быть один из трех: кобальтат лития LiCoO2, литий-феррофосфат LiFePO4, или литий-марганцевая шпинель LiMn2O4, а на медную фольгу наносят графит. Литий-феррофосфат LiFePO4 является единственным, на данный момент, безопасным катодным материалом с точки зрения опасности взрыва и экологичности в целом.
Полимерные электролиты, способные внедрять в свой состав соли лития, в силу своей пластичности делают возможным изготовление литий-ионных аккумуляторов с большой внутренней поверхностью и почти любой формы, а это значительно повышает как технологичность производства, так и массогабаритные характеристики.
В процессе заряда такого аккумулятора, ионы лития перемещаются через электролит, и внедряются в кристаллическую решетку графита на аноде, образуя соединение графитит лития LiC6. При разряде происходит обратный процесс – от анода ионы лития движутся к катоду (окислителю), а во внешней цепи к катоду движутся электроны, в результате процесс приобретает электрическую нейтральность.
Номинальное напряжение литий-ионного аккумулятора составляет 3,6 вольта, однако разность потенциалов при зарядке может достигать 4,23 вольта. В связи с этим фактом, заряд производится при максимально допустимом напряжении не более 4,2 вольта.
Некоторые соединения лития могут легко возгораться, если напряжение превышено, поэтому в литий-ионные батареи, традиционно, встраиваются контроллеры уровня заряда, не допускающие превышения критического напряжения. Еще одним способом обеспечения безопасности является встроенный клапан для сбрасывания избыточного давления внутри пакета.
Литий-ионные элементы всегда закрыты воздухонепроницаемой оболочкой, так как воздействие воды и кислорода в атмосфере может быстро повредить компоненты элемента.
В случае перезарядки или другого события, вызывающего повышение давления газа, устройство отключения тока изнутри отключает элемент от внешних подключений.
В призматических ячейках для этой цели часто используется диск, который выталкивается наружу из-за чрезмерного давления газа. К диску прикреплен положительно заряженный язычок, который в такой ситуации разрывает соединение. В цилиндрических звеньях сужение по окружности стенки звена позволяет ему удлиняться, что приводит к разрыву внутреннего соединения.
Ячейка иногда также включает в себя резистивный датчик температуры, сопротивление которого увеличивается с повышением температуры. Этот элемент имеет очень низкое (почти незначительное) сопротивление при комнатной температуре, а выше определенной температуры его сопротивление быстро увеличивается. Такие защиты могут быть встроены в ячейку, чтобы снизить риск термической нестабильности из-за внешних причин.
Смотрите также: Поченму взрываются литиевые аккумуляторы
Литий-ионные батареи уже заняли свое достойное место на рынке портативной бытовой техники. Это элементы питания сотовых телефонов, фотоаппаратов, видеокамер, планшетов, плееров, и т.д.
Моя статья на Яндекс Дзен:
Литий-ионные (Li-Ion) и литий-полимерные (Li-Pol) аккумуляторы - в чем отличие и что лучше?
Литий-феррофосфат LiFePO4 считается самым перспективным катодным материалом в силу своей экологичности. Кобальтат лития LiCoO2, в свою очередь, ядовит и экологически вреден, а у аккумуляторов на его основе лишь 50% ионов можно извлечь из структуры соединения, ведь если из него извлечь литий полностью, то структура станет нестабильной, кобальт перейдет в степень окисления +4 и сможет окислить кислород, а выделяющийся атомарный кислород станет окислять электролит, и произойдет взрыв. Аккумуляторы с повышенной емкостью (на основе LiCoO2) крайне взрывоопасны.
Литий-феррофосфат LiFePO4 был предложен в качестве катодного материала аккумуляторов для более мощных устройств в 1997 году Джоном Гуденафом.
Литий-феррофосфат есть в земной коре, и не создаст никаких экологических проблем в будущем. Из него не может выделяться кислород, так как он весь очень прочно связан фосфором с образованием устойчивого фосфат-иона. Однако, для возможности применения этого материала, его нужно было раздробить на мелкие частички, иначе он остался бы изолятором в силу очень малой проводимости. Частички сделали пластинчатыми с малыми размерами вдоль направления движения ионов лития, затем покрыли нанометровым слоем углерода.
Такие наночастицы LiFePO4 способны заряжаться за 10 минут, а если еще модифицировать покрытие, то время заряда сократится до 1-3 минут. В перспективе, именно этот материал сможет обеспечить питание электромобилей в течение 10 лет. Уже сейчас технологически возможен цикл зарядки-разрядки за 5-10 минут при полной безопасности.
С точки зрения современной науки, разработка и выпуск даже портативного наноаккумулятора не заставит себя долго ждать, и слово лишь за широким технологическим внедрением разработок. Что касается перспектив электромобилей, то сейчас уже можно считать, что именно они станут основным видом транспорта в городах ближайшего будущего.
Применение литий-ионных аккумуляторов:
Литиевые аккумуляторы в современных автомобилях
Правильная эксплуатация литий-ионных аккумуляторов
Самая большая литиевая аккумуляторная батарея в мире
Андрей Повный